脳動静脈奇形

脳血管奇形 (国際ガイドラインから)
H1: 専門委員会は、
オスラー病の疑い、または確定した成人の患者には、脳血管奇形のスクリーニングに、感度を最大限に高めるために、造影と非造影の検査や血液成分を検出する撮像法を用いたプロトコールのMRI検査を推奨します.
証拠のレベル III、(100%が同意)、推薦の強さ:弱い
H2: 専門委員会は、
脳血管奇形からの急性出血を呈する成人の患者には、神経血管病変の専門知意識を有する施設での決定的な治療を考慮することを推奨します.
証拠のレベル III、(94%が同意)、推薦の強さ:強い
H3: 専門委員会は、
脳血管奇形を持つその他の全ての成人患者は、神経血管病変に関する専門知識を有する施設に紹介し、侵襲的検査も考慮し、個別の管理を検討することを推奨します.
証拠のレベル III、(84%が同意)、推薦の強さ:強い
H4: 専門委員会は、
妊娠中に無症候性の脳血管奇形を持つことが分かったオスラー病の疑いまたは確診の妊婦は、脳血管奇形の最終的な治療を胎児娩出後まで延期することを推奨します.分娩の方法は、産科の原則に沿うことを推奨します.
証拠のレベル III、(80%が同意)、推薦の強さ:弱い
「国際HHTガイドライン第2版の臨床推奨事項と国際HHTガイドライン第1版の現在推奨されている臨床推奨事項について」Annals of Internal Medicine, 2020の和訳版から
HHT Q & A 50 から
Q1.動静脈瘻(どうじょうみゃくろう)・動静脈奇形・シャントなどの言葉がよく出て来ますが、どん なものか、説明してください.
A1. 血液は動脈-細動脈-毛細血管-細静脈-静脈の順に流れていますが(図1A)、動脈と静脈が正常の毛細血 管を介さずに直接つながってしまった状態を動静脈シャント(短絡)といいます.動静脈シャントは様々 な血管奇形で認められますが、その代表が動静脈奇形や動静脈瘻です.いずれも細静脈を含む毛細血管 の部分に病変があり、動静脈奇形は動脈と静脈がナイダスと呼ばれる異常血管を介してつながっており(図 1B)、動静脈瘻は直接つながっています(図1C).また動静脈瘻では短絡部の静脈が瘤状に拡張してい る(静脈瘤)ことが多いです.短絡部の手前の動脈を栄養動脈、すぐあとの静脈を流出(導出)静脈と 呼びます.動静脈瘻や動静脈奇形では毛細血管を介さないため血流は正常よりも速く、流出静脈には正 常よりも高い圧がかかっており、太く拡張しています.両者とも全身のどこにでもできますが、オスラー 病の患者さんでは肺、脳、肝臓に多く認められます.
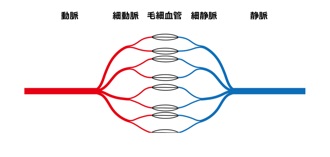
図1A: 正常血管のシェーマ. 血液は動脈-細動脈-毛細血管-細静脈-静脈の順に流れ ている
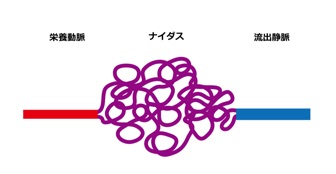
図1B: 動静脈奇形のシェーマ 動静脈奇形は動脈と静脈がナイダスを介してつながっ ている.
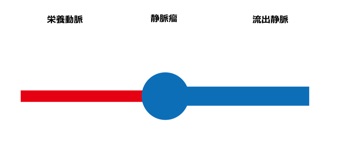
図1C: 動静脈瘻のシェーマ 動静脈瘻は動脈と静脈が直接つながっており、短絡 部直後には静脈瘤を認めている.
1. Whitehead KJ, et al: Arteriovenous malformtaions and other vascular malformation syndromes. Cold Spring Harb Perspect Med 3:a006635.doi:10.1101/cshperspect.a006635, 2013
Q2.なぜ、オスラー病の患者には、血管奇形ができるのですか?
A2. オスラー病の原因遺伝子であるendoglin、ACVRL1(ALK1)、SMAD4はいずれも血管新生やリモデリ ングを調節しているTGF-βシグナル伝達系に関与しています.遺伝子は父親からのものと、母親からの ものの一対からなっており、動物実験ではendoglinやACVRL1は一対の遺伝子の両方ともが変異している 場合(ホモ接合体)には胎児期に重大な血管発育不全が生じて致死的となります.一方、一対の遺伝子 のうち片方のみが変異している場合(ヘテロ接合体)ではヒトと同じ頻度ではありませんが、生後に毛 細血管拡張病変や動静脈奇形などの血管奇形が認められます.オスラー病に限らず血管奇形ができる詳 細な機序はまだ分かっていませんが、オスラー病ではendoglinやACVRL1遺伝子の片方の変異によって、 その遺伝子が作るタンパク質が不足するため十分に機能しない(ハプロ不全)ことで血管奇形が惹起さ れると考えられています.ただしオスラー病の患者さんでも全員に肺、脳、肝臓に動静脈奇形が形成され るわけではないので、遺伝子異常だけが原因ではなく環境要因も関与していると考えられています.
1. Whitehead KJ, et al: Arteriovenous malformations and other vascular malformation syndromes. Cold Spring Harb Perspect Med 3:a006635.doi:10.1101/cshperspect.a006635, 2013
2. Thomas JM, et al: Genetic and epigenetic mechanisms in the development of arteriovenous malformations in the brain. Clin Epigenetics 8:78 DOI 10.1186/s13148-016-0248-8, 2016
Q3. オスラー病はどのように診断するのですか?
A3. オスラー病の診断は臨床症状に基づくCuraçaoの診断基準に則って行われます. Curaçaoの診断基準
1. 繰り返す鼻出血
2. 皮膚・粘膜の毛細血管拡張病変 3. 肺・肝臓・脳・脊髄の動静脈奇形や動静脈瘻、消化管の毛細血管拡張病変 4. 第一度近親者(両親、兄弟(姉妹)、子供)にオスラー病の患者さんがいる
以上の4項目のうち、3項目以上でオスラー病の診断は「確実」、2項目で「疑い」、1項目以下で「否定 的」となります.16歳以降であれば、この診断基準でかなり正確に診断できます.オスラー病の子供さ んは繰り返す鼻出血や皮膚・粘膜の毛細血管拡張病変がまだ出現していないことが多いため、この診断 基準は適応されませんが、遺伝子検査を行えばオスラー病かどうか診断できます.正確には90%程度 で、遺伝子変異が認められますが、10%でオスラー病であるのもかかわらず遺伝子変異がみつかりませ ん.遺伝子検査で変異がみつかれば、子供さんでも重篤な合併症を起こす可能性がある肺や脳の動静脈 奇形があるかどうかをスクリーニングして、必要があれば予防的に治療を行うことが勧められます.遺伝 子検査は他に家族歴のない「疑い」例(発端者の可能性がある)に対しても有用です.現在の日本では オスラー病の遺伝子検査は保険適応がなく、保険診療で行うことができませんが、近い将来に認められ ると思います.
1. Shovlin CL, et al: Diagnostic criteria for hereditary hemorrhagic telangiectasia (Rendu-Osler-Weber syndrome). Am J Med Genet 91: 66-67, 2000
2. Komiyama M, et al: Hereditary hemorrhagic telangiectasia in Japanese patients. J Hum Genet 59: 37-41, 2014 3. McDonald J, et al: Hereditary hemorrhagic telangiectasia: genetics and molecular diagnostics in a new era. Front Genet 6: 1.doi:10.3389/fgene.2015.00001, 2015
Q4. オスラー病を診てもらうには、何科を受診すれば良いですか?
A4.オスラー病の患者さんは鼻出血なら耳鼻咽喉科、貧血や消化管出血なら内科、肺の動静脈瘻なら呼吸 器内科・呼吸器外科(胸部外科)や放射線科、脳の動静脈奇形や動静脈瘻なら脳神経外科・脳血管内治 療科と症状を出す臓器によって様々な診療科を受診する必要がありますし、遺伝に関する相談であれば 遺伝カウンセラーへの受診も有用です.しかし残念なことに各科の担当医師のすべてがオスラー病のこと を理解できていないのが現状です.したがってその病院(地域)でオスラー病の診療が可能で、症状に応 じて該当科へ紹介を調整してくれる医師を受診する必要があります.HHT JAPANのhome page (http:// komiyama.me/HHT_JAPAN/)またはNPO日本オスラー病患者会(https://www.hht.jpn.com)に医療 施設情報があるのでご参照ください)
Q5. 脳の血管奇形にはどのような治療法がありますか?
A5. オスラー病における脳の血管奇形は大きく脳動静脈瘻、脳動静脈奇形、毛細血管奇形の3つに分けら
れます.毛細血管奇形の頻度が最も高く、次いで脳動静脈奇形、脳動静脈瘻の順になります.
ナイダスのない脳動静脈瘻は小児、特に6歳以下で認められることが多く、治療法にはカテーテル手術 と開頭手術とがあります.カテーテル手術ではプラチナコイルや接着剤(アロンアルファー)などを用い て動脈と静脈の短絡部を閉塞します.一方、開頭手術では短絡部を金属クリップで遮断します.より低侵 襲であるカテーテル手術が選択されることが多く、症状を出していれば新生児でも行います.予定治療の 場合、カテーテル手術であれば約7-10日間の、開頭手術なら約14日間の入院となります.
ナイダスを伴う脳動静脈奇形は30歳頃に診断されることが多く、治療法には開頭手術、定位放射線治 療(ガンマナイフなど)、カテーテル手術があります.カテーテル手術は脳動静脈瘻と異なり完治より も短絡している血流量を落とす役割となることが多く、したがって前2者が主な治療法になります.出血 を起こした場合には再出血を予防するために開頭手術で病変の本体であるナイダスを切除・摘出するこ とが検討されます.しかしナイダスの部位や大きさなどから開頭手術のリスクが高いと判断した場合に は定位放射線治療が選択されます.定位放射線治療では正常脳に影響がない線量の放射線をナイダスに 向かって様々な方向から照射して、結果的にナイダスにのみ高線量の放射線が照射されます.小児では全 身麻酔が必要ですが、成人では局所麻酔での治療が可能です.しかし開頭手術とは異なり、その効果は ゆっくりとしか現れず、ナイダスが消失するのに約2-3年はかかりますし、完全に消失しないこともあり ます.脳動静脈奇形の出血によって半身麻痺や失語症などの神経症状を認める場合には病変の治療のほか にリハビリテーションが必要になります.出血を起こしていない脳動静脈奇形に対しては経過観察または 定位放射線治療が選択されることが多く、定位放射線手術は2泊3日の入院で受けることが可能で、退院 後すぐに学校や職場復帰できます.
毛細血管奇形は動静脈シャントを伴わない血管奇形で、大きさは10mm以下と小さなものです.出血を 起こすことはほぼないため、経過観察となります.
1. Krings T, et al: Neurovascular manifestations in hereditary hemorrhagic telangiectasia: imaging features and genotype-phenotype correlations. AJNR Am J Neuroradiol 36: 863-870, 2015
2. Faughnan ME, et al: International guideline for the diagnosis and management of hereditary haemorrhagic telangiectasia. J Med Genet 48: 73-87, 2011